БъЧЉЃК
НЈСЂСЫЪГЦЗАќзАИДКЯВФСЯжа2,4-ЖўАБЛљМзБНЕФGC-ECDМьВтЗНЗЈЁЃЗжЮіЬѕМўЮЊЃКHP-5УЋЯИЙмЦјЯрЩЋЦзжљ(30mЁС0.32mmЁС0.25ІЬm)ЃЛдиЦјСїЫй0.8mL/minЃЛНјбљПкЮТЖШЮЊ260oCЃЌЗжСїБШЮЊ5:1ЃЛECDМьВтЦїЮТЖШЃК300oCЃЛжљЮТЃК170oCЁЃНјбљСПЃК1ІЬLЁЃ2,4-ЖўАБЛљМзБНдк0.02mg/L~1mg/LЗЖЮЇФкЯпадСМКУЃЌЯрЙиЯЕЪ§ДяЕН0.9991ЃЌЗНЗЈМьГіЯоЮЊ0.001mg/LЁЃ
ЁЁЁЁ2,4-ЖўАБЛљМзБН(2,4-Diaminotoluene)ЪЧвЛжжгаЛњКЯГЩдСЯЃЌжЦШЁЕФМзБНЖўвьЧшЫсѕЅ(TDI)ЙуЗКгУгкИДКЯФЄДќЕФеГКЯЙЄвежаЁЃМзБНЖўвьЧшЫсѕЅМЋвзЫЎНтЃЌ-NCOЛсБфГЩ-NH2ЃЌЩњВњГЩ2,4-ЖўАБЛљМзБН[1]ЁЃбаОПБэУїЃЌ2,4-ЖўАБЛљМзБНЖдеГФЄЁЂКєЮќЕРМАЦЄЗєгаДЬМЄзїгУЁЃЮќШыЁЂЩуШыЛђОЦЄЗєЮќЪеПЩв§Ц№жаЖОЁЃЖЏЮяЪЕбщБэУїЦфЖдДѓЁЂаЁЪѓгажТАЉзїгУ[2]ЁЃ
ЁЁЁЁФПЧААќзАВФСЯжа2,4-ЖўАБЛљМзБНЕФВтЖЈЗНЗЈжївЊгаЦјЯрЩЋЦзЗЈ[3]ЁЂЦјжЪСЊгУвЧЗЈ[4]МАУЋЯИЙмЕчгОЗЈ[5]ЕШЁЃЮвЙњЁЖИДКЯЪГЦЗАќзАДќЮРЩњБъзМЁЗЃЈGB 9683—1988ЃЉжаЃЌЙцЖЈЖўАБЛљМзБН(4ЃЅввЫс)ЕФЯоСПвЊЧѓЮЊ0.004mg/LЃЛЁЖИДКЯЪГЦЗАќзАДќжаЖўАБЛљМзБНЕФВтЖЈЁЗЃЈGB/T 5009.119-2003ЃЉжаВЩгУGC-ECDЗНЗЈНјааМьВтЁЃЕЋдкЪЕМЪВйзїжаДцдквЛЖЈЕФШБЯнЃКЪзЯШБъзМжаВЩгУЖўТШМзЭщЮЊШмМСНјааБъбљХфжУЃЌгЩгкECDМьВтЦїЖдТБзхдЊЫиЗЧГЃСщУєЃЌвђДЫЕЭВаСєЕФЖўТШМзЭщШнвздьГЩМьВтЦїЕФЫ№ЛЕЃЛЦфДЮБъзМВйзїжаНЯЖрЕФзЊвЦЙ§ТЫВйзївздьГЩФПБъЮяЕФЫ№ЪЇЁЃБОЮФеыЖдЪЕбщВЛзуЮЪЬтНјааИФНјЃЌЪЙЦфОпгаНЯКУЕФВйзїадЁЃ
1 ЪЕбщВПЗж
1.1 жївЊвЧЦїгыЪдМС
ЁЁЁЁAgilent 7890AЦјЯрЩЋЦзвЧ(ИНЕчзгЗ§ЛёМьВтЦї,ECD)ЃЈАВНнТзПЦММгаЯоЙЋЫОЃЌУРЙњЃЉЃЛЕчШШКуЮТЙФЗчИЩдяЯфЃЈЩЯКЃЩаХЪЕбщвЧЦїгаЯоЙЋЫОЃЉЃЛа§зЊеєЗЂвЧ(ЩЯКЃЩъЩњПЦММгаЯоЙЋЫО)ЃЛ2,4-ЖўАБЛљМзБНЃЈDr.Ehrenstorfer GmbHmЃЌЕТЙњЃЉЃЛШ§ЗњввЫсєћ(TFAA) ѕЃЛЏЪдМСЃЈRegis ChemicalЃЌУРЙњЃЉЃЛМзБН(ЩЋЦзДП)ЃЛЖўТШМзЭщЃЈЩЋЦзДПЃЉЃЛЬМЫсЧтФЦЃЈЗжЮіДПЃЉЃЛЮоЫЎСђЫсФЦЃЈЩЋЦзДПЃЉЁЃ
ЁЁЁЁБъзМДЂБИвКЃКзМШЗГЦШЁ10mg 2,4-ЖўАБЛљМзБНЃЌгУЩЋЦзМЖМзБНЖЈШнжС100mLЃЌЕУ100mg/LБъзМДЂБИвКЁЃ
ЁЁЁЁБъзМЙЄзївКЃКЮќШЁвЛЖЈСПБъзМДЂБИвКЃЌвдМзБНЮЊШмМСЃЌж№МЖЯЁЪЭжСХЈЖШЮЊ0mg/LЁЂ0.1 mg/LЁЂ0.2 mg/LЁЂ0.5 mg/LЁЂ1 mg/LЁЂ5 mg/LЕФБъзМЙЄзївКЁЃ
1.2 ЦјЯрЩЋЦзЬѕМў
ЁЁЁЁЩЋЦзЬѕМўЃКHP-5УЋЯИЙмЦјЯрЩЋЦзжљ(30m×0.32mm×0.25μm)ЃЛдиЦјЮЊЕЊЦј(ДПЖШ≥99.999%)ЃЌСїЫй0.8mL/minЃЛНјбљПкЮТЖШЮЊ260ºCЃЌЗжСїБШЮЊ5:1ЃЛECDМьВтЦїЮТЖШЃК300ºCЃЛжљЮТЃК170ºCЁЃНјбљСПЃК1μL.
1.3 БъзМЧњЯпжЦзї
ЁЁЁЁЗжБ№ШЁ1mL2,4-ЖўАБЛљМзБНБъзМЙЄзївКгк50mLРыаФЙмжаЃЌМгМзБНВЙГфжС5mLЃЌдђБъзМШмвКХЈЖШЮЊ0mg/LЁЂ0.02 mg/LЁЂ0.04 mg/LЁЂ0.1 mg/LЁЂ1 mg/LЃЌИїМгШы60μLШ§ЗњввЫсєћЃЌГфЗжЛьдШЃЌжУгк30ºCКцЯфжаКуЮТЗДгІ30minЃЌШЁГіМгШы10mL NaHCO3ЃЈ20g/LЃЉГфЗжвЁдШЃЌОВжУЗжВуЃЌаЁаФЮќШЁЩЯВуМзБНВугк5mLШнСПЦПжаЃЌШнСПЦПжаЪТЯШМгШы5gЮоЫЎСђЫсФЦвдЮќШЁМзБНВужаЩйСПЫЎЗжЁЃ
1.4 бљЦЗДІРэ
1.4.1 ЮДзАЙ§ЪГЦЗЕФАќзАДќЃКгУеєСѓЫЎЯДШ§ДЮЃЌСмИЩЃЌАД2mL/cm2МЦЫузАШЫеєСѓЫЎЃЌШШЗтПкЁЃ
1.4.2 зАЙ§ЪГЦЗЕФАќзАДќЃКМєПкЃЌНЋЪГЦЗШЋВПвЦГіЃЌгУЧхЫЎГхЯДжСЮоЮлЮяЃЌдйгУеєСѓЫЎГхЯДШ§ДЮЃЌСмИЩАД2 mL/cm2МЦЫузАШыеєСѓЫЎЃЌШШЗтПкЁЃ
1.4.3 НЋЩЯЪі1.4.1Лђ1.4.2ШШЗтПкКѓЕФАќзАДќЃЌжУгкдЄЯШЕїжС100ºC±5ºCКцЯфФкЃЌКуЮТ60 minЃЌШЁГіздШЛЗХРфжСЪвЮТЃЌМєПЊЗтПкЃЌНЋЫЎвЦШЫИЩдяЕФЩеБжаБИгУЁЃ
1.4.4 бљЦЗВтЖЈЃКСПШЁБИгУЪдбљ50.0 mLЃЌжУгкЗжвКТЉЖЗжаЃЌгУ10 mLМзБНЗжБ№нЭШЁЖўДЮЃЌУПДЮнЭШЁ5 minЃЌОВжУ10 minЁЃКЯВЂЖўДЮнЭШЁвКЃЌдкЗжвКТЉЖЗЯТПкЗХИЩдяТЫжНЃЌвдБуГ§ШЅнЭШЁвКжаЫЎЗжЁЃНЋнЭШЁвКвЦШыK-DХЈЫѕЦїжаЃЌдк40ºCЫЎдЁжаХЈЫѕжСдМ2mLЃЌЗХРфЃЌМгШы60μLШ§ЗњввЫсєћЃЌЧсЧсЛьдШЃЌжУ30ºCКцЯфжаКуЮТЗДгІ30minЃЌАДЩЯЪіБъзМбљЦЗбмЩњЛЏКѓДІРэВНжшДІРэбљЦЗВЂНјааВтЖЈЁЃ
2 НсЙћгыЬжТл
2.1 Ш§ЗњввЫсєћгУСПЕФШЗЖЈ
2,4-ЖўАБЛљМзБНЪєгкИпЗаЕуЛЏКЯЮяЃЌвђДЫашвЊНјаабмЩњЛЏМьВтЃЌГЃгУЕФбмЩњЪдМСЮЊШ§ЗњввЫсєћ[3,6]ЃЌЗДгІЪНШчЭМ1ЫљЪОЁЃЭЈЙ§Ш§ЗњввЫсєћбмЩњЛЏМШПЩвдИФЩЦД§ВтЮяЕФЦјЯрЩЋЦзааЮЊЃЌвВЭЌЪБв§ШыСЫЕчИКадКмЧПЕФЗњЃЌШчЙћЦфСПКмДѓЃЌдђгаПЩФмНјШыгаЛњВуЃЌЫцзХ2,4вЛЖўАБЛљМзБНбмЩњЮяНјШЫЕчзгВЖЛёМьВтЦїдьГЩЮлШОЃЌвђДЫбмЩњМСЕФгУСПгІЪЪСПЁЃ
.png)
ЭМ1 2,4-ЖўАБЛљМзБНбмЩњЛЏЗДгІЪН
Fig.1 The derivatization reaction of 2,4-Diaminotoluene
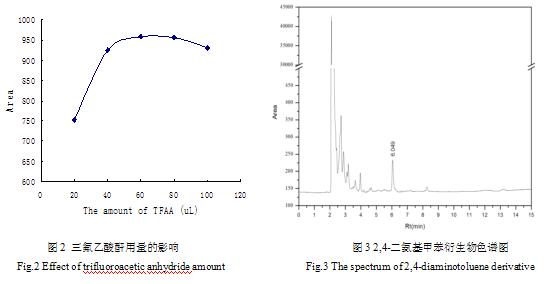
ЁЁЁЁдкШеГЃМьВтжаЃЌЖўАБЛљМзБНХЈЖШЖМВЛЛсИпгк1mg/LЃЌвђДЫШЁ5Зн1mL1mg/LБъзМбљЦЗгк50mLРыаФЙмжаЃЌМгМзБНВЙГфжС5mLЃЌЗжБ№МгШы20μLЃЌ40μLЃЌ60μLЃЌ80μLЃЌ100μLбмЩњМСНјаабмЩњЛЏЗДгІЃЌАД2.3ВНжшжаВйзїНјааВтЖЈЃЌЭМ2ЮЊВЛЭЌШ§ЗњввЫсєћгУСПЯТбмЩњЮяЕФЗхУцЛ§ЭМЃЌЭМ3ЮЊМгШы60μLШ§ЗњввЫсєћКѓбмЩњЮяЕФЩЋЦзЭМЃЌДгЭМПЩПДГіЃЌЫцзХШ§ЗњввЫсєћгУСПЕФдіМгЃЌЗхУцЛ§гаЫљдіМгЃЌ60μLКѓдіМгВЛУїЯдЃЌвђДЫБОЗНЗЈбЁгУ60μLШ§ЗњввЫсєћНјаабмЩњЁЃЯрБШНЯЙњБъжаБъзМШмвКбмЩњЛЏЫљгУЕНЕФ250μLШ§ЗњввЫсєћСПЃЌМДНкдМСЫЪдМСгУСПЃЌвВМѕЩйСЫбмЩњЛЏЪдМСДјРДЕФИЩШХЁЃ
2.2 ШмМСЕФбЁдё
ЁЁЁЁЙњБъбЁгУЖўТШМзЭщзїЮЊнЭШЁШмМСЃЌгЩгкЖўТШМзЭщКЌТБЫидзгЃЌЖдЦјЯрЩЋЦзЕФЕчзгВЖЛёМьВтЦїЫ№КІНЯДѓЁЃЭМ4ЮЊ1mg/LЕФ2,4-ЖўАБЛљМзБНЕФЖўТШМзЭщШмвККЭМзБНШмвКбмЩњЛЏКѓЩЋЦзЭМЃЌДгЭМПЩПДГіЃЌЖўТШМзЭщзїЮЊШмМСЪБЃЌШмМСЕФЯьгІжЕКмИпЃЌВњЩњСЫДѓЕФЭЯЮВЗхЃЌЕМжТ2,4-ЖўАБЛљМзБНбмЩњЮяВЛФмЪЕЯжЛљЯпЗжРыЃЌгАЯьВтЖЈЕФзМШЗадЁЃ
.png)
ЭМ4ВЛЭЌШмМСЬхЯЕЯТ2,4-ЖўАБЛљМзБНбмЩњЮяЩЋЦзЭМБШНЯЃК(1)ЃКЖўТШМзЭщЃЛ(2)ЃКМзБН
Fig.4 The comparasion of 2,4-Diaminotoluene derivative spectrμm in different solventЃК(1): Dichloromethane; (2): Toluene
2.3 ЯпадЗЖЮЇМАМьГіЯо
ЁЁЁЁЙњБъжажЛжЦБИ—ИіЖўАБЛљМзБН-Ш§ЗњввЫсєћБъзМЙЄзївКЃЌСйгУЪБдйЯЁЪЭГЩВЛЭЌЕФХЈЖШВтЖЈЛцжЦБъзМЧњЯпЃЌетжжЗНЗЈДцдквЛЖЈШБЯнЃЌШчБъзМШмвКжЦБИЁЂбмЩњЛЏЙ§ГЬеЦЮеВЛЕБОљЛсдьГЩаЃзМЯпЕФЮѓВюЃЌДгЖјгАЯьЖЈСПЕФзМШЗадЁЃБОЮФжЦБИвЛЯЕСаБъзМЙЄзївКНјаабмЩњЛЏВтЖЈЃЌИљОнБъзМШмвКХЈЖШКЭЗхУцЛ§ЛцжЦБъзМЧњЯпЁЃ2,4-ЖўАБЛљМзБНЕФБъзМЧњЯпЯпадЗНГЬЮЊЃКy=2318.1x+24.091ЃЌЯрЙиЯЕЪ§R2ЮЊ0.9991ЃЌдк0.02mg/L~1mg/LЗЖЮЇФкЯпадСМКУЁЃИљОн3БЖаХдыБШМЦЫуМьГіЯоЃЌвЧЦїМьГіЯоЮЊ0.01mg/LЃЌЛЛЫуЕНбљЦЗжаПЩЕУГіЗНЗЈМьГіЯоЮЊ0.001mg/LЁЃ
2.4 ЛиЪеТЪгыМьГіЯо
ЁЁЁЁЛиЪеТЪЪЧЗДгІД§ВтЮядкбљЦЗЗжЮіЙ§ГЬжаЕФЫ№ЪЇЕФГЬЖШЃЌЫ№ЪЇдНЩйЃЌЛиЪеТЪдНИпЁЃШЁвЛЗнПеАзбљЦЗЃЌМгШывЛЖЈКЌСПЕФ2,4-ЖўАБЛљМзБНЃЌЭЈЙ§ЩЯЪівЧЦїЬѕМўНјааЗжЮіЁЃИљОнНЈСЂЕФБъзМЧњЯпЖЈСПЃЌМЦЫубљЦЗЕФМгБъЛиЪеТЪ, ЯрЭЌЬѕМўЯТВтЖЈ6 ДЮЃЌШЁЦфЦНОљжЕНјааМЦЫуЃЌНсЙћШчБэ3ЫљЪОЁЃМгБъЛиЪеТЪдк94.40%~102.37%жЎМфЃЌЯрЖдБъзМЦЋВюдк2.43%~5.36%жЎМфЁЃ
Бэ1 бљЦЗМгБъЛиЪеТЪ
Table.1 The resμLt of sample recovery
|
Added
(ug)
|
Found
(ug)
|
Recovery (%)
|
RSD
(%)
|
|
0.2
|
0.2053 0.2021 0.1857 0.1992 0.2110 0.2010
|
100.36
|
4.21
|
|
0.5
|
0.4997 0.5139 0.5092 0.4973 0.5219 0.5292
|
102.37
|
2.43
|
|
2
|
2.0011 1.8194 2.0008 1.8182 1.9079 1.7731
|
94.40
|
5.36
|
2.5 ЪЕМЪбљЦЗМьВт
ЁЁЁЁИљОн2.4жабљЦЗДІРэЗНЗЈЖдШеГЃбљЦЗНјаа2,4-ЖўАБЛљМзБННјааМьВтЃЌбЁШЁ30ИіХњДЮЕФИДКЯЪГЦЗАќзАДќНјааДІРэЃЌНсЙћ2ИібљЦЗМьГіЃЌЧвОљаЁгкЙњБъЕФЯожЕЃЌЦфгрбљЦЗОљЮДМьГіЃЌЫљНЈСЂЕФЗНЗЈФмгІгУгкШеГЃМьВтЙЄзїжаЁЃ
3 НсТл
ЁЁЁЁБОЮФеыЖдЁЖИДКЯЪГЦЗАќзАДќжаЖўАБЛљМзБНЕФВтЖЈЁЗ(GB/T 5009.119-2003)БъзМжаЕФВЛзужЎДІМгвдИФНјЃЌЭЈЙ§ЖдШмМСбЁдёЃЌбмЩњЮягУСПЃЌнЭШЁВНжшМђЛЏЕШЗНУцНјааЬжТлЃЌНЈСЂСЫЖўАБЛљМзБНЕФGC-ECDВтЖЈЗНЗЈЃЌЗНЗЈМьГіЯоЮЊ0.001mg/LЁЃИУЗНЗЈгаНЯКУЕФСщУєЖШКЭбЁдёадЃЌТњзуЪГЦЗАќзАИДКЯВФСЯжа2,4-ЖўАБЛљМзБНЕФВтЖЈвЊЧѓЁЃ
ВЮПМЮФЯз
[1] YI Juan(вз Оъ)ЃЌZHANG Xue-kui(еХбЇ). Modern Preventive Medicine(ЯжДњдЄЗРвНбЇ)[J], 2007, 34(18):3541.
[2] LIU Xue-li (СѕбЉРђ). Foreign Medical Sciences(Section Hygiene)(ЙњЭтвНбЇ(ЮРЩњбЇЗжВс))[J], 1981, (2):103.
[3] LI Shao-xia(РюЩйЯМ)ЃЌHUANG Wei-xiong(ЛЦЮАал)ЃЌLV Feng(ТР Зв)ЃЌCHEN Ming(ГТ Уї)ЃЌZHONG Xiu-hua(жгауЛЊ)ЃЌHUANG Jing-chu(ЛЦОАГѕ). Food Science(ЪГЦЗПЦбЇ)[J], 2013, 34(8):240.
[4] MA Ming(Тэ Уї)ЃЌZHOU Yu-yan(жмгюбо)ЃЌZHOU Yun(жм дЯ)ЃЌCHEN Yu-xiao(ГЬгћЯў)ЃЌQing Jiang(Чх Н)ЃЌZHANG Kai(еХ П). Chinese Journal of Analysis Laboratory(ЗжЮіЪдбщЪв)[J],2013, 32(6):50.
[5] ZHONG Yan-qin(жгбоЧй)ЃЌZHANG Jing(еХ ОВ)ЃЌHU Jie-lan(КњНрРМ)ЃЌLI Yong-xin(РюгРаТ)ЃЌSUN Cheng-jun(ЫяГЩОљ). Chinese Journal of Analysis Laboratory(ЗжЮіЪдбщЪв)[J],2014, 33(6):729.
[6] MA Ming(ТэУї),ZHOU Yu-yan(жмгюбо),Qing Jiang(ЧхН),Liu Shu(СѕЪя),ZHANG Kai(еХП). Environmental Chemistry(ЛЗОГЛЏбЇ) [J],2012, 31(12):2018.
ЃЈНвѕЪаВњЦЗжЪСПМрЖНМьбщЫљЁЁКњНЈЃЉ